悪性胸膜・腹膜中皮腫の発生率、治療及び生存:人口ベース研究/Kooten JP et al. Thorax 2022;77:1260–1267
抄録
はじめに:悪性中皮腫(MM)は、主に胸膜(MPM)または腹膜(MPeM)に発生する侵襲性の強いがんであり、その大部分はアスベスト曝露に起因する。本研究では、1993年の全国的なアスベスト禁止以降における、オランダの人口ベースの発生率、治療及び生存についてレビューした。
材料及び方法:1993年から2018年に診断されたMPMまたはMPeM患者をオランダがん登録から選択した。(年齢別及び性別の)改訂欧州標準化発生率(RESR)について年間変化率(APC)を算出した。治療パターン及びカプラン・マイヤー法による全生存時間解析を実施した。
結果:本研究には合計12,168例の患者が対象となった。80歳以下の男性患者において、MMの発生率は過去10年間で有意に減少した(APCは-9.4%から-1.8%の範囲、p<0.01)。80歳超の男女患者では、研究期間全体を通じて発生率が有意に増加した(APCは各々3.3%及び4.6%、p<0.01)。2003年以降、全身化学療法の使用が、とくにMPMについて(9.3%から39.4%に)増加した。全体として、患者の62.2%は抗腫瘍治療を受けていなかった。抗腫瘍治療を受けなかった主な理由は、患者の希望(42%)及びパフォーマンスステータス(25.6%)であった。全生存期間中央値は、1993~2003年の7.3か月から、2004~2011年には8.9か月、2012~2018年には9.3か月へと改善した(p<0.001)。
結論:オランダにおけるMMの発生率は2010年頃にピークに達し、現在ではほとんどの年齢層で減少傾向にある。全身化学療法の使用が2003年以降増加しており、これが時間の経過とともに全生存率の改善につながったと考えられる。しかしながら、大多数の患者は治療を受けておらず、予後は依然として不良である。
主要メッセージ
主要な問いは何か?
→1993年の全国的アスベスト禁止は、悪性中皮腫の発生率にどのような影響を与えたのか?また、治療法の進歩はオランダにおける中皮腫の予後にどのような影響を与えたのか?
結論は何か?
→悪性中皮腫の発生率は、オランダの全国的アスベスト禁止後、予想よりも約10年早くピークに達した。
→治療法の進歩により生存率は多少向上したものの、予後は依然として厳しい。
読むべき理由は?
→これらの知見は、アスベスト規制が従来の予想よりも早期に中皮腫発生率の減少をもたらすことを示しており、悪性中皮腫の大部分は効果的に予防可能であるという考えを支持するものである。
→12,000人以上の中皮腫患者で観察された治療パターン及び生存結果は、より優れた中皮腫治療法の必要性が依然として存在することを浮き彫りにしている。
はじめに
悪性中皮腫(MM)は、主に胸膜に発生し、次いで腹膜に発生する致死率の高い腫瘍である。散発性症例では、心膜または精巣鞘膜に由来する場合もある。悪性胸膜中皮腫(MPM)は、全MM症例の90%以上を占める。MPMの予後はきわめて不良であり、化学療法による治療時の中央生存期間(OS)は約1年である。最近、ニボルマブ(抗PD-L1抗体(PD-1))及びイピリムマブ(抗CTLA-4抗体 (CTLA4))からなる併用チェックポイント阻害療法が、標準的な第一選択化学療法と比較して、MPM患者のOSを延長することが示されている(OS中央値 18.1か月 vs 14.1か月)。この結果を受け、アメリカ食品医薬品局(FDA)は、切除不能MPMに対する第一選択治療としてニボルマブとイピリムマブの併用を承認した。悪性腹膜中皮腫(MPeM)の場合、OS中央値は約6か月である。長年にわたり、治療選択肢はMPMと同一であった。2009年以降、複数の研究により、選択されたMPeM患者において減量手術(CRS)と温熱腹腔内化学療法(HIPEC)を併用することで、長期生存が達成可能であることが示されている。
MPM発症の主なリスク要因はアスベスト曝露である。この相関関係は、MPeMではやや顕著ではない。アスベスト曝露とMMの決定的な関連性は、1960年にWagnerらによって証明された。この発見にもかかわらず、アスベストの生産量は1970年から1980年にかけて世界的にピークを迎え、年間400万トン以上に達した。オランダにおけるアスベスト使用量もこの時期にピークを迎えた。新たな規制によりその後10年間で使用量は減少したが、オランダでアスベスト全面禁止が実現したのは1993年であった。ロシア、カザフスタン、中国などの国々は、今日でもアスベストの大規模生産国であり、他の国々ではごく最近になって使用が禁止されている。潜伏期間(すなわちアスベスト曝露からMM診断までの期間)には10年から50年以上と報告されているように大きなばらつきがあるため、将来のMM発生率を予測することは困難である。オランダではMM死亡率のピークは2020年頃と予測されていた。本人口ベース研究は、全国的なアスベスト禁止から25年後の全国MM発生率をレビューする。これは、他国がアスベスト規制実施後のMM発生率を予測するうえで参考となり得る。同時に、MPMとMPeMの両方について、発生率、MMの特性、治療及び生存におけるパターンを確認することを目的とする。
方法
データの収集
1993年から2018年の間にMMと診断された患者は、オランダがん登録(NCR)において、胸膜(C38.4)または腹膜(C48.2)に位置するICD-Oコード8000~8005、 9050~9053及び9990(国際疾病分類腫瘍学第3版第1改訂版)の症例を検索することによって確認した。発生率は1989年から2018年まで入手可能であった。データはNCRモニタリング委員会及びNCR肺腫瘍学科学委員会の承認を得て抽出された。データは最新の欧州プライバシー規制(一般データ保護規則、欧州連合2016/679)にしたがって取り扱われた。オランダでがんと診断された全患者のデータはNCRによって収集される。De Boerらが以前、その方法を記述している。要約すると、NCRは、オランダ病理解剖学全国自動化アーカイブ及び全国病院退院診断登録簿を用いてがん患者を確認している。専門の職員が診療記録から診断、病期、治療に関する情報を収集する。生存状況に関する情報は、全国自治体個人記録データベースを通じて年次更新されている。生存状況は2020年2月1日時点で更新済みである。データ抽出及び研究者への提供は、研究チームに属さない訓練を受けた者によって実施された。
腫瘍ステージは全患者について登録された。MPMについては、診断時点における腫瘍、リンパ節、転移(TNM)分類が用いられた。MPeMについては、Surveillance Epidemiology and End Results(SEER)に基づく疾患範囲(EOD)コーディングが用いられた。EODコーディングは、腫瘍ステージを局所進行、限局進行、遠隔進行に分類する。NCRでは、一般的な病期分類システムが利用できない場合にこれを使用する。転移部位は、2008年以降に特定された。死亡原因は、個人情報保護規制により入手できなかった。
発生率分析
1989年から2018年までの発生率を分析した。年齢別及び性別の発生率は、改訂欧州標準率(RESR)を用いて算出した。発生率の傾向を確認するために、SEER「ジョインポイント回帰プログラム」(V.4.8.0.1、2020年4月)を使用した。このソフトウェアは、発生率にもっとも単純な回帰モデルを当てはめることで、傾向の断絶、いわゆる「ジョインポイント」を確認する。ジョインポイントは、モンテカルロ順列検定を用いて決定した。年間変化率(APC)は、診断年を独立変数とし、発生率の自然対数を用いてデータに対数線形回帰モデルを適合させることで本ソフトウェアにより算出された。APCは、2つのジョインポイントの期間、またはジョインポイントがゼロの場合は全期間にわたって算出された。
治療パターン分析
治療は傾向分析のために、全身化学療法、手術、放射線療法及びベストサポーティブケアの4つの主要カテゴリーに階層化された。手術には、減量手術、CRS、胸膜剥離術及び胸膜外肺切除術など複数の処置が含まれた。その他の治療カテゴリーは、血管新生阻害剤ベバシズマブ、チロシンキナーゼ阻害剤(データではさらなる詳細は未記載)、抗PD(L)-1及び抗CTLA4薬剤であるニボルマブ、ペンブロリズマブ、イピリムマブからなるチェックポイント阻害剤を含む、標的療法及び免疫療法であった。治療戦略は、MPMについては年ごとに、MPeMについては5年ごとにレビューされた。2015年以降は、抗腫瘍療法を受けなかった理由が記録された。
生存分析
生存傾向を定義するために、データを3つの期間に階層化した。第1期間は1993年から2003年までに診断された症例、第2期間は2004年から2011年までの症例、第3期間は2012年から2018年までに診断された症例で構成された。2003年が意図的に選択されたのは、Vogelzangらがシスプラチンとペメトレキセドの併用化学療法に関する第Ⅲ相治験の結果を、この年に発表したためである。その後の年は、生存率の改善を評価するため2等分した。異なる疾病ステージで診断されたMPM患者の生存率を比較するために、2007年に改訂された第7版TNM病期分類マニュアルが採用された2008年以降のデータのみを用いた。MPeMについては、広く用いられている疾病ステージ分類システムが存在しないため、疾病ステージ比較は行わなかった。また、異なる治療法(化学療法、手術及び「ベストサポーティブケア」)ごとの生存率を示すために、カプラン・マイヤー生存曲線も作成したが、これらの結果は(選択)バイアスに大きく影響されるため、意図的に統計的比較は行わなかった。
統計解析
連続変数は中央値と四分範囲(IQR)で示され、独立標本中央値検定で比較した。分類変数は、頻度と割合で示され、χ2検定で比較した。生存解析は、カプラン・マイヤー法を用いて実施した。群間の生存期間は、比例ハザードの場合にはログランク検定、非比例ハザードの場合には一般化ウィルコクソン検定で比較した。両側検定のp値が0.05未満の場合を統計学的に有意とみなした。統計解析は、「Statistical Package for Social Sciences」(SPSS)V.25.0.0.1及びR V.4.0.2(http://www.r-project.org)を用いて実施した。発生率はSAS V.9.4で算出した。
結果
患者及び腫瘍の特徴
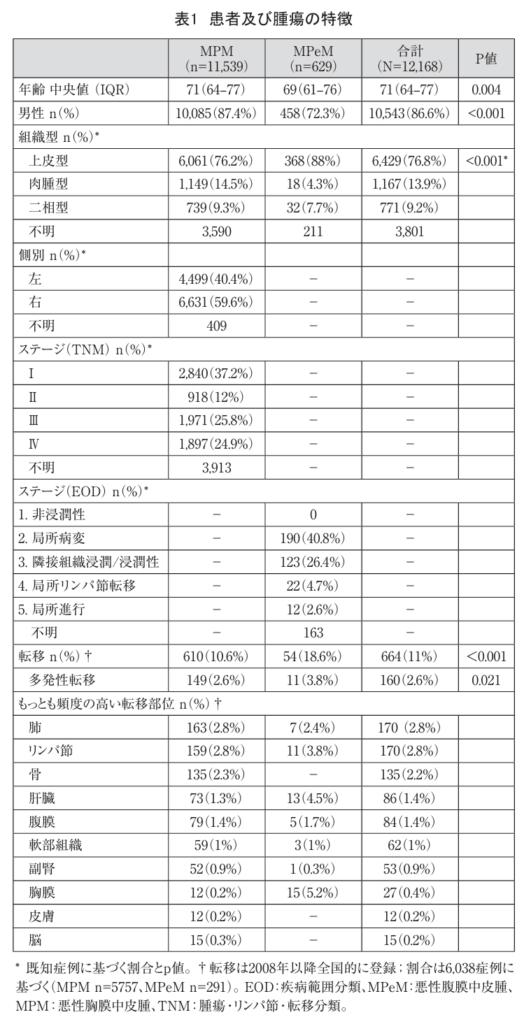
1993年から2018年の間にNCRで確認されたMM患者は12,168例であった。このうち11,539例(94.8%)がMPM、629例(5.2%)がMPeMであった。診断時の患者及び腫瘍の特徴に関する包括的な概要を表1に示す。一般的に、MPeM患者は若年であった(中央値年齢69歳(61~76歳) vs 71歳(64~77歳)、p=0.004)。MPM群では男性患者がより多く(87.4% vs 72.3%、p<0.001)。さらに、MPeM患者では上皮様型サブタイプがより多く認められた(88% vs 76.2%、p<0.001)。病理学的サブタイプの発生傾向を時系列で検出する試みは、病理学的登録データの不足により失敗した。ただし、サブタイプが病理医によってより詳細に特定される傾向が明らかになった。研究期間の最初の10年間では症例の46.7%であったが、最後の10年間では83%に増加した(オンライン補足図1)。両腫瘍タイプで異なる疾病ステージ分類システムが使用されたため、MPMとMPeM間の比較は不可能であった。また、診断時の疾病ステージについて傾向を特定する試みは、疾病ステージ不明症例数が多いため失敗した。本分析では、研究期間中に疾病ステージ分類の使用がわずかに増加したことが明らかになったが、依然として約3分の1の患者で疾病ステージが記録されていない(オンライン補足図2)。
発生率
研究期間中、男女合計のMM発生率は、10万人年当たり2.6~4.1人年(RESR)の範囲であった(補足表A)。発生率は、2010年まで年1.6%(95%信頼区間 1~2.1)で有意に増加したが、その後は年-1.7%(95%信頼区間 -3.9~0.6)の非有意な減少または横ばい傾向が観察された。
MPMについては、発生率は、1989年から2007年にかけて年間1.8%(95%信頼区間1.1~2.5)の割合で増加し、10万人年当たり2.4~3.5人年(RESR)の範囲であった。2007年以降は、有意ではない減少が認められ(APC=-1%、95%信頼区間-2.5~0.4)、発生率は10万人年当たり3.3~3.8例(RESR)の範囲であった(図1)。
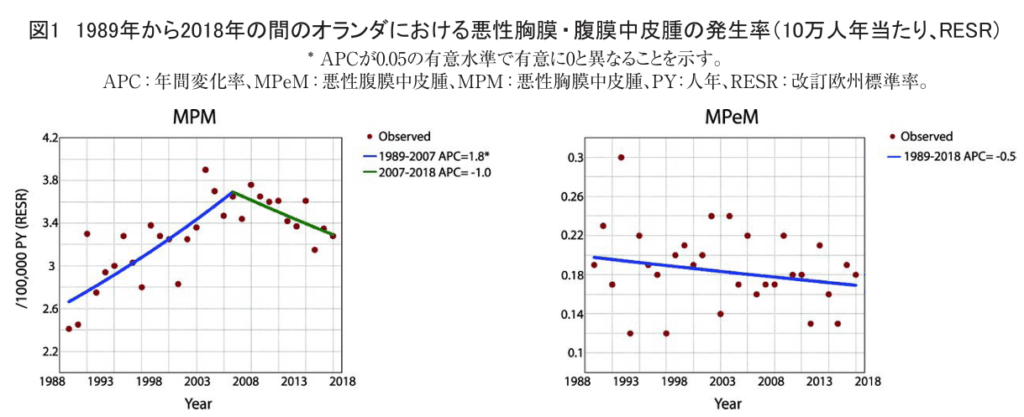
MPeMについては、研究期間全体を通じて年10万人年当たり約0.15~0.25人年(RESR)が報告された(図1)。有意な傾向は認められなかった(APC=-0.5、95%CI -1.4~0.4)。男性の発生率が10万人年当たり0.2~0.5例(RESR)の範囲であったのに対し、女性の発生率は10万人年当たり0~0.2例(RESR)の範囲であった。
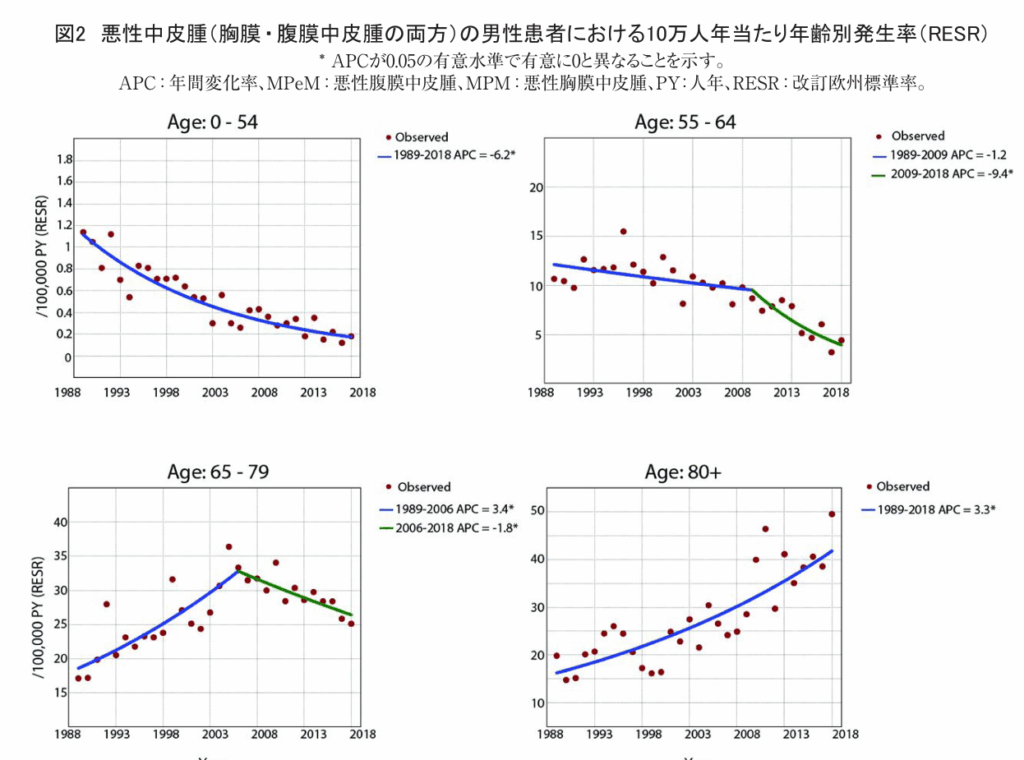
MPeMのみについての年齢別発生率は入手できなかったため、MPMとMPeMを合わせて、性別及び年齢別発生率の分析を実施した。男性患者では、80歳超の患者群を除く全年齢層でMM発生率が有意に減少した。80歳超の患者群では、研究期間全体で発生率が上昇し、平均年平均変化率(APC)は3.3%(95%信頼区間 2.5~4.1)であった(図2)。0~54歳の男性患者では、1989年から2018年にかけて年平均6.2%の減少が認められた(95%CI -7.2~-5.2)。55~64歳の男性患者では、2009年から2018年にかけて有意な発生率の減少が認められた(APC=-9.4%、95%CI -13.1~-5.4)。65~79歳の男性患者では、1989年から2006年にかけて有意な増加(APC=3.4%、95%CI 2.3~4.5)が認められた後、2006年から2018年にかけて有意な減少(APC=-1.8%、95%CI -3.5~-0.1)が観察された。65歳未満の女性患者では、MM発生率に有意な傾向は認められなかった。65歳以上の女性患者では、研究期間全体を通じて発生率の有意な増加が認められた(65~79歳のAPC=1.8%、95%CI 0.9~2.6、80歳以上のAPC=4.6%、95%CI 2.2~6.9)(補足表B及びC)。
治療
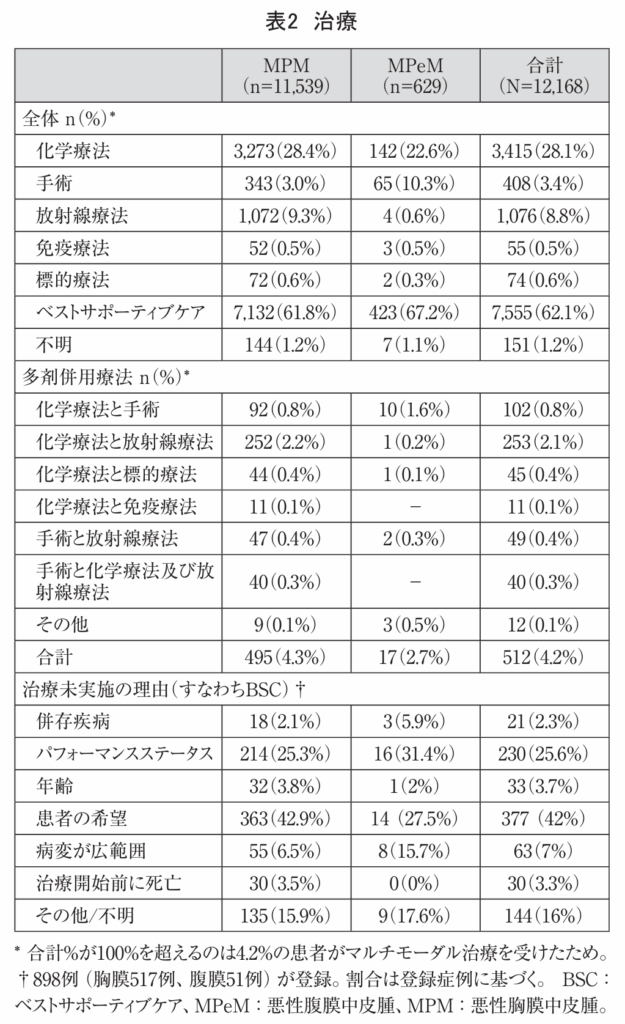
治療法の包括的な概要を表2に示す。1993年から2018年まで、MM患者の大多数(62.1%)が「ベストサポーティブケア」を受けた。2015年以降、抗腫瘍治療を受けなかった理由が898例の患者で記録された。大半の症例では、患者の希望(42%)またはパフォーマンスステータス(25.6%)が理由であった。MM患者の28.1%に化学療法、8.8%に放射線療法が、3.4%に何らかの外科手術が施行された。手術の目的が肉眼的完全切除であったか、またそれが達成されたかについての情報は登録されていない。MM患者のうち、4.2%がマルチモダリティアプローチによる治療を受けた。標的療法は74症例(0.6%)、免疫療法は55症例(0.5%)で用いられた。
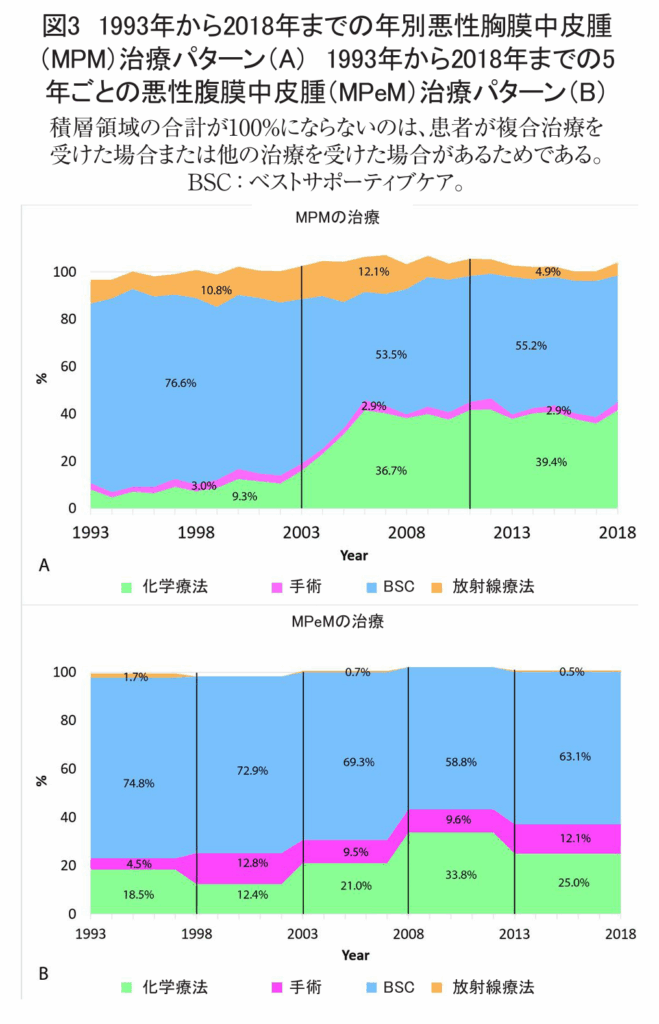
MPM患者では、MPeM患者と比較して化学療法(28.4% vs 22.6%)及び放射線療法(9.3% vs 対0.6%)の施行頻度が高かった。一方、手術はMPeM患者(10%)においてMPM患者(3%)よりも頻繁に施行された。図3Aは、MPMに対する全身化学療法の使用率が2002年から2006年にかけて年間約10%から40%に増加したことを示している。2006年以降、MPM治療における化学療法の使用率は安定していた。放射線療法は、2008年まで症例の約10~15%で使用されたが、その後は年間4~5%に減少した。図3Bが示すように、MPeM患者では、ベストサポーティブケアがもっとも一般的な治療法であった。その使用率は、1993年から1997年にかけて約75%、2013年から2018年にかけて約65%の範囲で推移した。化学療法の使用率は、2003年頃から増加し、2008年から2012年にピークを迎えた後、再び減少した。手術の役割は、研究対象期間中は限定的であり、5年ごとの割合は4%から13%の間で変動した。
生存
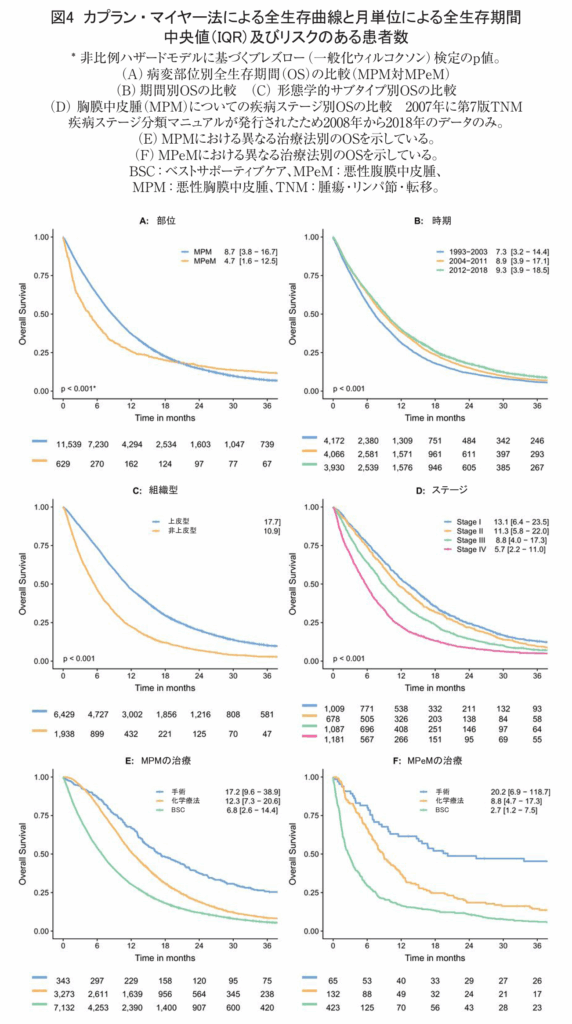
コホート全体における全生存期間(OS)の中央値は8.4か月(IQR[四分位範囲]:3.6~16.6か月)であった。異なるサブグループにおける中央生存期間を示すカプラン・マイヤー曲線を図4に示す。MPeM患者は、MPM患者と比較して中央生存期間が劣っており(4.7か月 vs 8.7か月、p<0.001)、全身化学療法を受けた場合においても同じであった(8.9か月 vs 12.7か月、p<0.001;データ未提示)。コホート全体の生存率は、2003年頃から有意に改善しており、これは、併用化学療法の導入及びこの治療使用率の増加によるものと考えられる。2012年から2018年までの間の全患者についてのOS中央値が9.3か月であったのに対して、1993年から2003年までの間は7.3か月であった。非上皮様形態(すなわち二相型及び肉腫型組織型)の患者は、予後が有意に不良であり(5.5か月 vs 9.2か月、p<0.001)、全身化学療法を受けた場合においても同じであった(8.9か月 vs 13.6か月;データ非提示)。中皮腫(MPM)については、疾病ステージによりOSに有意差が認められた(2008から2018年のデータ)。ステージIと診断された患者の中央生存期間が13.1か月(IQR 6.4~23.5)であったのに対し、ステージIVの患者では5.7か月(IQR 2.2~11.0)であった。図4E、Fは、それぞれMPM及びMPeMについての、化学療法、手術及び「ベストサポーティブケア」についての生存率を示している。これらの結果は、選択バイアスが作用しているため、統計的に比較はしなかった。
討論
本研究は、オランダにおいてほとんどの年齢層でMMの発生率が現在減少傾向にあることを示している。MM発生率のピークは2010年頃に過ぎたようであり、現在では人口全体に対して発生率が減少する強い傾向が認められる。歴史的に、オランダは比較的高いMM発生率を有する国のひとつであった。最近数十年間、MM発生率の急激な増加が懸念をもって監視されてきた。先行研究では、オランダにおける中皮腫の影響及び死亡率を予測しようとしてきた。今回初めて、更新された発生率データを用いて、本研究は、オランダのほとんどの年齢層でMM発生率が減少していることを観察した。同様の結果は、スウェーデン、アメリカ、オーストラリアでも以前に報告されている。イギリスなど、アスベスト使用を禁止したMM発生率の高い他の国々においても、これらの知見は、将来のMM発生率予測にさらに役立つ可能性がある。
これらの知見は注目に値する。なぜなら、オランダにおける発生率は2020年頃にピークに達すると予測されていたからである。しかし、このピークはすでに2010年頃に到達している。これは、MM発生率がアスベストの完全禁止だけでなく、1993年以前に実施された対策とも関連していることを示唆している。1969年に発表されたJ Stumphius(オランダの造船所の産業医)の論文は、オランダにおけるアスベスト曝露と中皮腫の関連性を明確に示した。この論文は追加研究につながり、最終的に1978年の政府規制につながった。その結果、1980年代のオランダにおけるアスベスト加工量は、1970年代と比較して約75%減少した。1980年以降、アスベストの加工・使用量が急減し、また、中皮腫の潜伏期間が平均30年であることを考慮すると、2010年以降の発生率減少は、予測可能であった。これはまた、1993年のアスベスト完全禁止以前に、55歳未満の患者における発生率がすでに減少傾向にあった理由を説明するものでもある。
本研究で分析された年齢別発生率は、80歳超の男性患者及び65歳超の女性患者を除き、ほとんどの年齢層におけるMPM発生率が現在減少傾向にあることを示している。アスベスト曝露からMM発症までの潜伏期間を考慮すれば、こうした観察結果は予想どおりである。現在80歳超の患者は、過去に(職業的に)アスベストに重度に曝露した可能性が高い。しかし、その他の全年齢層の男性における現在の発生率低下は、新規MM症例数が近い将来さらに減少すること、そして、ピーク発生率はすでに過ぎ去ったことを示唆している。1993年のアスベスト禁止措置及びそれ以前の対策により、アスベストに重度に曝露された患者集団は年々縮小している。80歳超集団は相対的に高い発生率を示すが、集団規模は毎年減少中である。したがって、この年齢層が総発生率に占める比重は低下している。他の全年齢層における発生率低下と相まって、これが現在のMM総発生率減少をもたらしている。
MPeMについては、患者数が少ないため、年齢別発生率は得られなかった。しかし、MPeM全体については、発生率は時間経過とともにほぼ安定していた。これは、アスベスト曝露とMPeMの関連性がMPMほど強くないことを示唆している可能性がある。また、過去の放射線治療や生殖細胞変異など、MPeM発症のより支配的な他の原因が存在することを示唆している。本コホートにおけるMPeMの割合は5.2%であった。これは、文献で報告されている10~30%の範囲より低い値である。ただし、MPeMは誤診されやすいことが知られており、本コホートでの低頻度は、この誤診率を反映している可能性がある。
治療に関しては、2002年から2006年にかけて全身化学療法の使用が顕著に増加し、とくにMPM治療で顕著であった。2003年、Vogelzangらは、MPMにおいてシスプラチン単独療法と比較してプラチナ製剤-ペメトレキセド併用療法が全生存期間(OS)の中央値を3か月延長することを示した。治療率の増加が、併用療法が生存期間を延長するという事実と相まって、2003年以降、集団レベルでの生存率の改善につながったと考えられる。
しかし、患者の大半は、抗腫瘍治療を受けていなかった。抗腫瘍治療を受けなかったMPM患者では、40%以上が患者の希望によるものだった。おそらく、患者は毒性の強い治療、とくに効果が限定的な場合には、その実施を望まないのだろう。ベルギーやイギリスでも同様の傾向が見られている。MPeM患者では、パフォーマンスステータスの低下(31.4%)や進行した病態(15.7%)がより頻繁に理由として挙げられた。MPeM患者は、その病気の希少性と非特異的な症状のために、進行した段階で診断されることが多いことが知られている。
MPMに対する放射線療法の使用は一般的であったが、2009年頃に減少した。この背景には、2008年に更新された欧州臨床腫瘍学会(ESMO)のガイドラインが関係している。同ガイドラインは、放射線療法の潜在的な重篤な副作用を考慮し、その使用を局所的緩和療法及び疼痛管理に限定すべきであると述べている。一方で、局所病変制御におけるその有益性については議論の余地がある。2016年及び2019年には、予防的管腔照射の有益性の欠如がランダム化試験で確認された。これらの結果により、その使用はさらに減少する可能性がある。
現在のコホートでは、免疫療法及び標的療法の使用、ひいてはその影響はごくわずかであり、いずれかの治療法を受けた患者は1%未満であった。これは、チェックポイント阻害療法がまだ治療選択肢として承認されておらず、標的療法に関しても大きな進展がなかったためである。最近、第Ⅲ相CheckMate 743治験の結果が発表され、初回治療としてMPM患者に対するチェックポイント阻害療法の併用療法が、標準的な初回化学療法と比較してOSを4か月延長することが示された。非上皮型サブタイプでは、生存期間の利益はさらに大きかった。このサブタイプでは、免疫療法群の2年生存率推定値は38%であったのに対して、化学療法群では8%であった。この結果を受け、FDAは、MMの第一選択治療としてニボルマブ+イピリムマブの併用療法を承認した。ただし、MMに対する単剤療法は、特定の患者層に有効な場合があるため、完全に否定すべきではない。とはいえ、患者の生存率向上には新たな治療選択肢が依然として緊急に必要とされている。新たな進展の概要はYapらによって示されている。われわれのグループは、胸膜及び腹膜中皮腫における樹状細胞療法に取り組んでいる。
MMに対する外科手術の役割は依然として議論の的である。現在のコホートではその使用は最小限であり、外科的治療を受けたのはMPM患者のわずか3%、MPeM患者の約10%のみである。とくにMPeM患者については、これは機会を逃した可能性が高い。MPeMに対するCRS-HIPECの使用に関する複数の症例報告が発表されている。例えば、Yanらによる大規模な症例報告では、中央生存期間が53か月、3年生存率60%、5年生存率47%が観察された。この生存率は患者選択によって部分的に説明できる。しかし、全身化学療法に関する研究も患者選択の影響を受けるが、長期生存例を示すことは稀である。
強みと限界
われわれの研究の強みは、データを収集した対象患者数及び期間の長さである。議論すべき限界も存在する。大多数の地域ベース登録と同様に、限界の根本的な問題はデータの詳細にある。例えば、MPMの疾病ステージは、診断時に使用されたTNM分類に基づいて記録された。1993年から2018年にかけて異なるTNM分類が使用されたため、診断時の病期を時系列で比較することは困難であった。さらに、患者の約3分の1には疾病ステージが記録されていなかった。これは、オランダにおけるMPMに対する外科手術の適用がきわめて限定的であったためと考えられる。したがって、病理学的TNMステージ(pTNM)はほとんど欠如しており、全身化学療法がゴールドスタンダードとみなされているため、臨床的TNMステージ(cTNM)は、治療方針に影響を与えない。全身化学療法の患者選択は、疾病ステージよりも主にパフォーマンスステータス及び患者の希望に基づいて行われる。また、治療に関する詳細情報が欠落しているケースが多かった。生存分析に関しては、プライバシー規制によりNCRでは死因が登録されていない。したがって、がん特異的生存率は利用できなかった。
しかし、MMの予後がきわめて不良であることを考慮すると、高齢患者であっても、これが、われわれの結果に影響を与えた可能性はきわめて低い。これらの限界により、異なる疾病ステージ及び治療法間の生存率に関する詳細な追加分析は困難となったが、2010年以降のオランダにおける発生率の減少傾向を示すわれわれのデータの主要な結論に影響を与えることはなく、また、治療法の経時的傾向にも影響を及ぼさなかった。
結論
本研究は、1993年のアスベストの全国的禁止後、オランダにおけるMMの発生率が2010年頃にピークに達したことを示している。現在、80歳超の男性患者及び65歳超の女性患者を例外として、ほとんどの年齢層で、MM発生率は減少傾向にある。治療を受けた患者数は2003年以降増加しているが、大半の患者は抗腫瘍療法を受けていない。この期間に生存率はわずかに改善したものの、予後は依然として不良である。近年の治療法の進歩により、この認識が変わる可能性がある。
※https://thorax.bmj.com/content/77/12/1260
安全センター情報2026年4月号


